Hoe vaak gebeurt het dat je iets kunt toevoegen aan de studieboeken? Het lukte twee Nederlandse onderzoeksgroepen: in een bijzondere gelijktijdige publicatie beschrijven ze verschillende ontdekkingen rond transcriptie en herstel van DNA-schade.
‘Ik sprak met Martijn Luijsterburg over een screen die hij had gedaan naar factoren die betrokken zijn bij DNA-schade. Hij had een veelbelovende hit. Dat is mooi, zei ik, als het maar niet ELOF1 is! Want die hadden we net zelf opgepikt. Maar dat was het dus wél.’ Jurgen Marteijn vertelt lachend hoe zijn onderzoeksgroep aan het Erasmus Medisch Centrum en Oncode Instituut en die van Martijn Luijsterburg aan het Leids Universitair Medisch Centrum besloten de handen ineen te slaan toen ze ontdekten aan hetzelfde eiwit te werken. Dat pakte goed uit, want vorige maand publiceerden beide groepen hun vondst in twee zogenoemde back-to-back publicaties in Nature Cell Biology (Luijsterburg en Marteijn, met een New & Views redactionele bespiegeling).
Hun publicaties draaien om de rol van het eiwit ELOF1 bij TC-NER, een vorm van herstel van DNA-schade tijdens transcriptie. ELOF1 blijkt een cruciale schakel om de DNA-hersteleiwitten te wijzen waar ze moeten zijn. ‘Het is de matchmaker tussen het enzym en het substraat’, stelt Luijsterburg.

‘In afwezigheid van ELOF1 leidt een probleem met transcriptie óók tot problemen in de replicatie.’
Martijn Luijsterburg
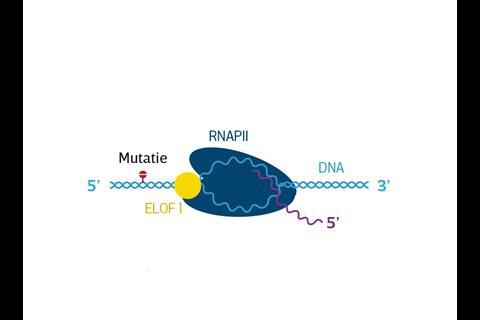
Transcriptie is de naam van het proces waarbij specifieke delen van het DNA – genen – worden afgelezen, wat verschillende stukjes RNA oplevert. Deze RNA-transcripten dienen vervolgens als instructie voor het maken van eiwitten. Het was al bekend dat ELOF1 onderdeel is van RNA polymerase II (RNAPII), het eiwitcomplex dat deze transcriptie verzorgt. Als zogenoemde elongatiefactor is ELOF1 medeverantwoordelijk voor de synthese van RNA-transcripten.
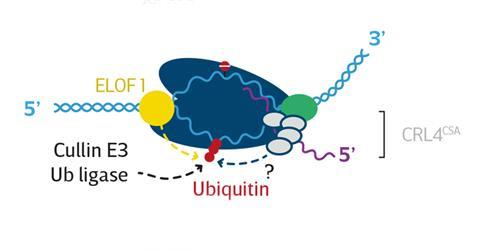
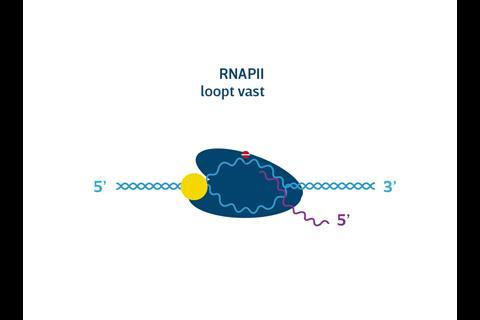
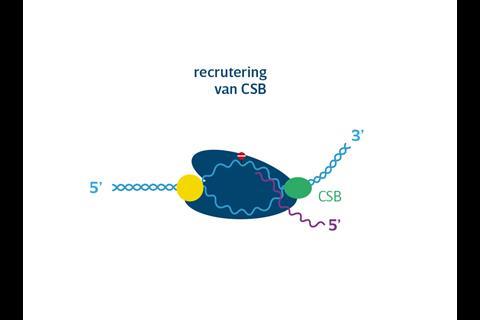
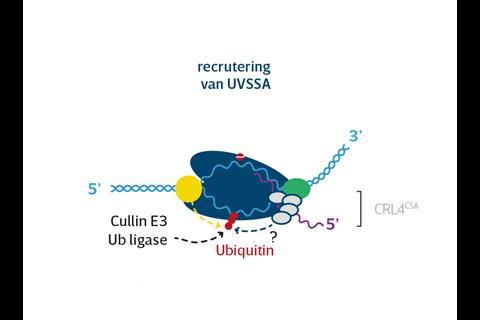
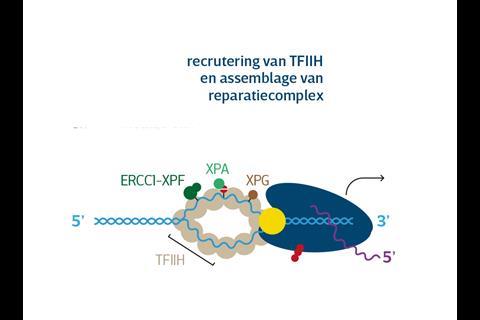
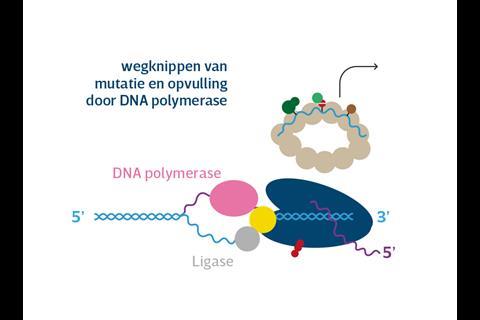
‘De RNAPII-trancriptiemachinerie heeft grote problemen met beschadigingen in het DNA, bijvoorbeeld veroorzaakt door uv-straling of toxische stoffen’, vertelt Marteijn. ‘Het loopt erop vast.’ Maar de cel heeft vernuftige methodes om DNA-schade al tijdens transcriptie te repareren en ELOF1, zo blijkt uit het onderzoek van Marteijn en Luijsterburg, speelt daarbij een cruciale rol. ‘Als RNAPII vastloopt op een beschadiging, landen de eiwitten CSA, CSB en UVSSA op het transcriptiecomplex’, legt Marteijn uit. ‘We wisten al dat die ervoor zorgen dat er een marker, een ubiquitine-peptide, aan RNAPII wordt gekoppeld die aangeeft dat er DNA-schade is die gerepareerd moet worden. Tegelijk met Martijn Luijsterburgs groep vonden we dat ELOF1 daartussen de cruciale schakel vormt.’ ELOF1 dirigeert het ubiquitine namelijk naar precies de juiste plek – lysine 1268 – aan de voorkant van RNAPII. Dit vormt het signaal voor DNA-hersteleiwitten als UVSSA en TFIIH om aan de slag te gaan.
Er is ook een tweede manier waarop DNA wordt afgelezen: replicatie. Hierbij wordt het volledige DNA in één keer gekopieerd omdat de cel zich in tweeën deelt. Replicatie en transcriptie worden door compleet verschillende systemen verzorgd, maar ze kunnen elkaar wel in de weg gaan zitten als er ergens schade is in het DNA, vertelt Marteijn. ‘De replicatiemachinerie merkt kleine schade nauwelijks op en gaat er gewoon overheen. Maar als het tijdens het kopiëren een vastgelopen RNAPII-complex tegenkomt, dan gaat het mis.’ Marteijn vergelijkt het met een geschaarde vrachtwagen die alle rijbanen blokkeert. Zo’n transcriptie-replicatieconflict leidt tot breuken in het DNA en uiteindelijk tot celdood.

’Als de replicatiemachinerie tijdens het kopiëren een vastgelopen RNAPII-complex tegenkomt, gaat het mis.’
Jurgen Marteijn
Luijsterburg en Marteijn hebben aanwijzingen dat ELOF1 ook een rol speelt in een nog onbekende, alternatieve DNA-herstelroute. Luijsterburg: ‘We weten dat het eerste reparatieproces volledig afhangt van het CSB-eiwit. Maar in cellen die al deficiënt zijn in CSB, zien we tijdens DNA-replicatie een extra probleem ontstaan als we dan ook ELOF1 weghalen. En dat verwacht je niet als beide eiwitten in dezelfde pathway zouden functioneren.’
Een mogelijke verklaring die beide onderzoekers opperen is dat ELOF1 ervoor zorgt dat vastgelopen RNAPII niet botst met de DNA-kopiëereiwitten tijdens DNA-replicatie. ‘Maar zeker weten doen we het nog niet, daar hopen we de komende tijd achter te komen’, besluit Luijsterburg.
Cockayne syndrome
Zonder ELOF1 kun je niet leven, wat iets zegt over het belang van dit eiwit. Mutaties in andere eiwitten in hetzelfde TC-NER pathway, zoals CSA en CSB, leiden tot Cockayne Syndrome, een zeldzame erfelijke ziekte die een direct gevolg is van het feit dat DNA-schade – vaak door uv-straling – tijdens transcriptie niet meer kan worden gerepareerd. Patiënten lijden onder meer aan versnelde veroudering, falende organen en neurologische problemen, en worden gemiddeld slechts acht jaar.



















Nog geen opmerkingen