Specifieke nanokristallen op een inerte drager nodig? Door te spelen met zoutoplossingen kun je er bakken vol van maken, laat Wim Noorduin zien.
Leren hoe de natuur zelfassemblage organiseert, en nieuwe functionele materialen maken door zulke processen waar nodig bij te sturen. Dat is waarmee Wim Noorduin, groepsleider self-organizing matter binnen het Amsterdamse NWO-instituut AMOLF, zich onder meer bezighoudt. In Advanced Materials presenteerde hij samen met Hans Hendrikse en Arno van der Weijden onlangs zijn nieuwste product: silicabloempjes als dragers van nanokristallen naar keuze, die bijvoorbeeld kunnen dienen als heterogene katalysator.
Chemische tuin
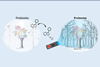
Het recept lijkt op dat van een klassieke chemische tuin met kristallijne ‘bomen’ in waterglas, een natriummetasilicaatoplossing. Maar Noorduin legt uit dat zo’n tuin vooral bestaat uit silica, waarin metaalionen opgesloten zitten. ‘Dat proberen wij juist te voorkomen. Wij willen dat die ionen carbonaatkristallen vormen met CO2, dat vanuit de lucht naar binnen diffundeert. Silica vormt zich daar omheen als een soort matrix.’
Onder bepaalde condities levert het fraaie bloemvormige structuren op. Voor het eerst haalden die de media in 2013, toen Noorduin nog werkte bij de groep van Joanna Aizenberg aan de Harvard University. Sindsdien heeft hij rekenmodellen ontwikkeld die aardig duidelijk maken wat er gebeurt. ‘Diffusiesnelheden bepalen de vormen en de pH speelt daarbij een grote rol. Door kleine, lokale concentratieverschillen worden ze niet allemaal identiek. We kunnen dat steeds beter sturen. Om het nog beter te begrijpen, werken we samen met wiskundigen die zich specialiseren in de groei van koraal. Dat mechanisme werkt anders, maar we kunnen wel delen van de modellering gebruiken.’
Als je eenmaal weet hoe het moet, is het een simpel proefje. Maar het lijkt alleen te lukken met calcium, barium en strontium. Andere metaalionen leveren gewoon een chemische tuin op. ‘Zelfassemblage berust op feedbackmechanismes die we nog maar gedeeltelijk begrijpen’, verzucht Noorduin.
In 2018 lukte het een kalkskelet van een zee-egel te voorzien van een perovskietlaagje, en inmiddels laten ook de in silicaat verpakte kristallen zich chemisch omtoveren. Met zoutoplossingen kun je calcium omruilen voor zowat elk overgangsmetaal dat een stabiel carbonaat kan vormen. En zodra dat proces helemaal is afgerond (een harde voorwaarde) laten ook de carbonaationen zich makkelijk vervangen. Zo kun je magnetisch Fe3O4 creëren of katalytisch actief NiO.
Het kristalrooster blijft hetzelfde, en ook de vorm van de kristallen verandert niet. Het volume wel, maar de silicaatschil blijkt flexibel genoeg om dat op te vangen. In elk geval in het begin: Noorduin vertelt dat sommige studenten het experiment niet konden reproduceren, omdat ze te langzaam werkten, terwijl het silicaat verder uithardde.
Scepsis wegnemen
Vooral het katalytische aspect trekt inmiddels de aandacht. Nanodeeltjes die uit een inerte drager steken, zijn hot in die hoek. Het is een totaal ander vakgebied dan zelfassemblage: om te beginnen doe je typische katalyse-experimenten niet met een handvol bloempjes, maar eerder met een paar gram materiaal. ‘Dus hebben we van die bakken besteld waarin ze op congressen de warme lunch opdienen. Binnen een week hádden we grammen’, grinnikt Noorduin.
En mede dankzij die bulkproductie weet hij de aanvankelijke scepsis van katalytici meestal snel weg te nemen. ‘Zodra we een sample hebben opgestuurd, bellen ze op en zeggen: bizar, het werkt zó goed…’
Voor publicatie Hendrikse et al. (2020) Advanced Materials 32(52) zie hier.














Nog geen opmerkingen