Twee artikelen van een Amsterdamse groep geven inzicht in elektrochemische routes voor ‘groene moleculen’. ‘Als je deze processen naar industriële schaal wilt overbrengen, moet je de route begrijpen.’
Zeg je elektrochemie, dan zeggen veel mensen ook direct ‘groen’. Als je het vergelijkt met traditionele organische of katalytische chemie, wat geeft het die groene eigenschappen dan? ‘Vooral als je het over de energietransitie hebt, is het groen in de zin dat je elektrochemische reacties kunt aansturen met enkel elektronen’, zegt Amanda Garcia, universitair docent aan de Universiteit van Amsterdam. ‘Je hebt geen hoge temperatuur of druk nodig, en je kunt de reacties meestal in water uitvoeren, hoewel we ook kijken naar vriendelijkere organische oplosmiddelen.’ Een voorbehoud is natuurlijk dat de elektronen een duurzame oorsprong moeten hebben, bijvoorbeeld opgewekt door windmolens of zonnepanelen.
Onlangs publiceerde de groep van Garcia twee artikelen – in JACS en ChemCatChem – over het synthetiseren van nuttige verbindingen op een groenere en duurzamere manier. ’Hoewel ze inhoudelijk heel verschillend zijn, worden alle reacties aangedreven door elektronen onder omgevingsomstandigheden.’
Goedkoop
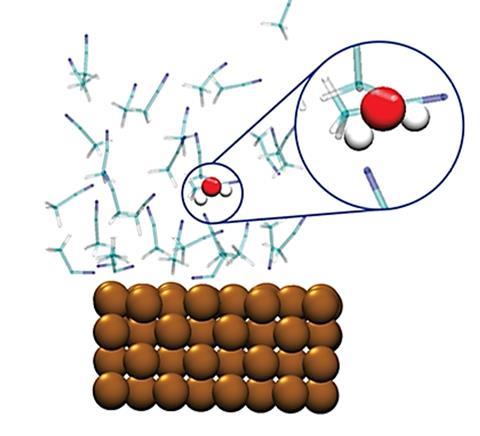
In ChemCatChem belichten Garcia en haar team een veelvoorkomend probleem met de CO2-reductiereactie (CRR). ‘De energie die je in het systeem stopt, wordt deels verbruikt door een parasitaire reactie om waterstof te produceren’, zegt Garcia. Het probleem ontstond toen ze met organische oplosmiddelen gingen werken, waardoor het reactiemechanisme van de CRR veranderde. ‘Organische oplosmiddelen bevatten altijd een zeer kleine hoeveelheid water. Deze paar parts-per-million zijn genoeg om het reactiemechanisme te veranderen in de richting van het waterstofproduct. We hebben een aantal simulaties uitgevoerd om te zien op welk moment dit mechanisme dominant wordt.’ Daaruit blijkt dat water een voorkeursinteractie heeft met de koperelektrode, meer dan de acetonitril die ze gebruikten. Een gouden tip is dus om je oplosmiddelen heel goed te drogen.
Het belangrijkste idee dat de onderzoekers in JACS poneerden is de elektrochemische vorming van koolstof-stikstofverbindingen. ‘We waren benieuwd of dit mogelijk was en besloten te proberen formamiden te maken’, legt Garcia uit. ‘Dit soort verbindingen hebben veel toepassingen en tot nu toe was het erg moeilijk om ze te maken zonder metaalkatalysatoren. Hier laten we zien dat het kan met een goedkope glasachtige koolstofelektrode.’
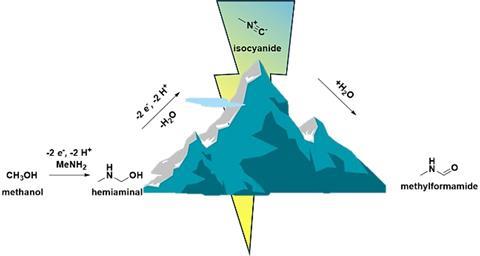
‘Een grote verrassing was dat we methylisocyanide, een zeer giftige chemische stof, veilig konden maken’, vervolgt Garcia. ‘Daarom kwam het ook in JACS. Een van de commissieleden zei tegen ons: “Jullie hebben een heel goedkoop en eenvoudig mechanisme gevonden om precies te doen waar ik naar zocht!” Hoewel ik er niet zeker van was dat ik dit tijdschrift wilde proberen, was promovendus Pim Broersen, die het experiment ontwierp, volledig overtuigd en hij had helemaal gelijk.’
Cruciaal
Op deze manier opent elektrochemie de mogelijkheid om waardevolle chemicaliën te synthetiseren op manieren die vaak ontoegankelijk zijn via traditionele organische of katalytische chemie. Maar waarom werkt het? In beide artikelen gebruikte het team van Garcia geavanceerde elektrochemische methoden om het mechanisme achter de elektrochemische reacties te onderzoeken. ‘We gebruiken in situ spectroscopische technieken om de belangrijkste tussenproducten te identificeren, vaak stabiele radicalen. Als je eenmaal weet wat zich tijdens het proces vormt, wordt het gemakkelijker om andere reacties te ontwerpen.’
Het is een cruciale stap die vaak over het hoofd wordt gezien. ‘Mensen kijken vaak alleen naar het eindproduct en dat is op zich prima, maar als je deze processen naar industriële schaal wilt brengen, moet je de route begrijpen om de opbrengst te verhogen.’
Elektrochemie is hier ideaal voor omdat het veel controle biedt. ‘Om een reactie af te tunen, kun je de stroom of spanning aanpassen. Dat is veel flexibeler dan bijvoorbeeld het afstellen van de druk; veel industriële processen werken al met een hoge druk, die moeilijk verder af te stellen is. Maar elektrochemie is anders, het is heel gevoelig en je kunt precies regelen hoeveel lading er door het systeem gaat.’
Broersen, P.J.L. et al. (2025) JACS 147(12), DOI: 10.1021/jacs.4c16725
Deacon-Price, C. et al. (2025) ChemCatChem 17(6), DOI: 10.1002/cctc.202401332
















Nog geen opmerkingen