De synthese van vitamine B12, nu vijftig jaar geleden, was een waar hoogstandje waar synthetisch chemici hun handen vol aan hadden. Maar de wetenschap achter deze bijzondere vitamine gaat nog veel verder terug.
Wat is er eigenlijk zo speciaal aan vitamine B12? Het is de enige vitamine die kobalt bevat, vandaar ook de minder gangbare benaming cobalamine, en kent de laagste ADI, advanced daily intake, van alle vitaminen, namelijk 3 µg. Maar het bijzondere zit vooral in de structuur. B12 heeft de meest ingewikkelde structuur van de vitaminen, die bovendien niet voorkomt in het plantenrijk en uitsluitend wordt geproduceerd door bacteriën die in symbiose leven met hogere organismen.
Vitaminen worden ontdekt in de tijd van Louis Pasteur, toen ziekten nog toegeschreven werden aan de aanwezigheid van een exogeen agens. In 1890 bewijst de Nederlandse microbioloog Martinus Beijerinck echter dat ziekte ook kan ontstaan door afwezigheid van een nutritionele factor. Maar het verhaal van B12 begint nog eerder, in 1849. De Britse arts Thomas Addison beschrijft in dat jaar een dodelijke bloedarmoede, pernicieuze anemie, maar hij vindt geen remedie.

Lever
Bijna tachtig jaar later, in 1925, toont de Amerikaanse patholoog George Whipple aan dat kalfslever werkt tegen de anemie bij honden, wat in 1926 ook wordt aangetoond in mensen door George Minot en William Murphy. De drie krijgen in 1934 de Nobelprijs voor Fysiologie of Geneeskunde voor deze ontdekkingen. In 1928 uit William Castle, Amerikaans fysioloog, het vermoeden dat een extrinsieke factor (EF) in de voeding (hier: lever) en een intrinsieke factor (IF) uit het maagslijmvlies samen voor deze tegenactie verantwoordelijk zijn. Pas in 1948 wordt een rode kristallijne substantie uit de lever geïsoleerd en geïdentificeerd als een variant van de EF. De substantie wordt later geïdentificeerd als cyanocobalamine. In 1955 slaagt de Britse scheikundige, en latere Nobelprijswinnaar, Dorothy Hodgkin, er met behulp van de X-stralendiffractie in om de structuur te bepalen. Het is voor de eerste keer dat de structuur van een biomolecule uitsluitend met die techniek wordt opgehelderd.
‘Door een “competitieve samenwerking” zegevieren de onderzoekers na bijna twaalf jaar’
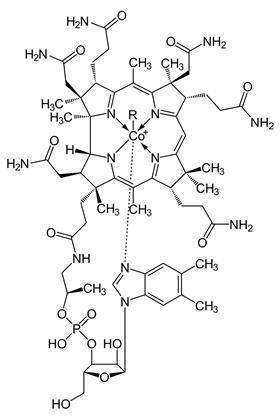
Over die structuur is heel wat te vertellen. Het gaat om een corrine-ring; een cyclisch tetrapyrrool, verwant aan de porfyrine-ring. In het midden van de ring is het sporenelement kobalt gebonden aan de vier N-atomen van de pyrrool-moleculen. Aan de onderkant van deze ring is de kobalt verbonden met een zijketen via een benzimidazool. Het andere uiteinde van de zijketen, dat fosfor bevat, is bevestigd aan één van de pyrrolen van de corrine-ring. Bovenaan de ring en loodrecht op het kobaltatoom staat één van de vier R-groepen die de variëteit van B12 bepaalt.
Huzarenstuk
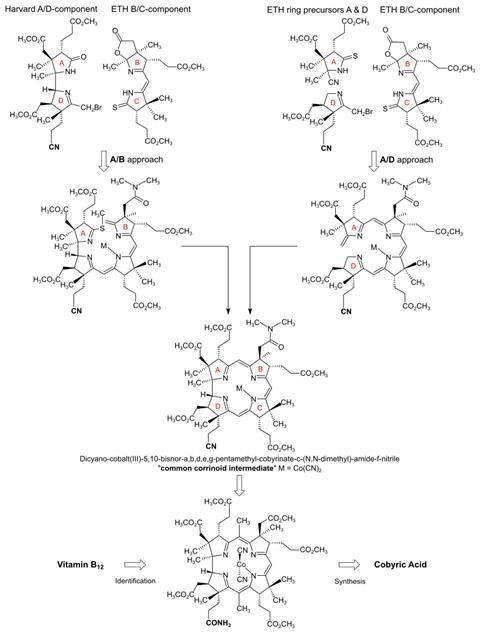
Zodra de structuur van B12 bekend is begint de wedloop naar een synthetische route. Die blijkt enorm ingewikkeld, met maar liefst 72 stappen waarin vele reactietypes een plaats hebben, waaronder Grignard, Diels-Alder, Birchreductie, diazomethaan en ozonolyse. De belangrijkste stappen op een rijtje (zie ook de afbeelding onderaan):
- pyrrolen A en B bereiden door resolutie (fysiek scheiden)
- pyrrolen C en D bereiden uit chiraal startmateriaal
- A en D samenvoegen
- koppelen aan B – C stuk
- kobalt inbrengen
- laatste cyclisering
Een ongekend complexe synthese die voor kleine bacteriën echter geen enkel probleem levert!
Maar de synthese lukt uiteindelijk door de gezamenlijke inspanning van de labo’s van Robert Woodward (Harvard), die in 1965 de Nobelprijs voor Scheikunde voor zijn eerdere werk kreeg, en Albert Eschenmoser (ETH Zürich) met 91 postdoctoraal en 12 PhD-studenten. Door een ‘competitieve samenwerking’, gebruikmakend van meest briljante chemische synthese van die periode, zegevieren de onderzoekers na bijna twaalf jaar. De weg naar het eindproduct blijkt al even gecompliceerd als de molecule zelf.
Oost, west…
De beide groepen begonnen initieel los van elkaar rond het begin van de jaren zestig. B12 is ingedeeld in een ‘westelijk deel’ en een ‘oostelijk deel’, die beiden twee ringen bevatten. West heeft ring A en D, Oost bevat B en C; samen vormen de vier ringen de corrine-ring. Om tot die corrine-ring te komen hebben Woodward en Eschenmoser verschillende strategieën bedacht. Enerzijds was er de gecombineerde Harvard/ETH methode, waarbij Harvard het AD-fragment synthetiseerde en ETH het BC-fragment. Dan koppel je ring C aan ring D en sluit je de corrine-ring met een basereactie. Tegelijkertijd was Eschenmoser ook bezig met een alternatieve strategie: wederom maakten ze het BC-fragment, maar nu maakten ze ook de twee losse ringen A en D. Die sloot zijn team aan op het BC-fragment en koppelde daarna op fotochemische wijze ring A en D aan elkaar. Beide methodes eindigen met de corrine-ring die de twee groepen vervolgens verder modificeerden tot het eindproduct, wat uiteindelijk lukt in 1972.
Fysiologie en functie van B12 in het menselijk lichaam
De opname van B12 uit de voeding in het bloed gebeurt door het ileum, het laatste deel van de dunne darm, dankzij het complex EF + IF, gevormd hogerop in het maagdarmkanaal. Dit complex wordt vervoerd naar de cellen voor zijn werking; naar de lever voor opslag (in grote voorraad) en voor uitscheiding in de gal en de feces. De EF is niets anders dan B12 en IF is een glycoproteïne, aangemaakt en afgescheiden door het maagslijmvlies. Zonder IF geen complexvorming, geen resorptie, geen deugdelijke erytrocyten ofwel rode bloedcellen (2,5.106 per seconde!). Zonder B12 treedt vorming op van reuze-erytrocyten van korte levensduur en dus bloedarmoede.
B12 fungeert als coenzym in twee reactietypes: de transmethylaties en isomerisaties. De variant methyl-B12 (R = -CH3) helpt de katalyse van de transmethylatie in het cytoplasma. Dit is de verhuis van de methylgroep naar een andere molecule, zoals in de reactie van homocysteïne naar methionine. Deze omzetting is belangrijk in de eiwitsynthese. In de mitochondriën is een andere variant, adenosyl-B12, actief. Hier is R = deoxyadenosylradicaal dat, indien veresterd met fosfaatgroepen, een rol speelt in de energiehuishouding van de cel via AMP, ADP, ATP. Adenosyl-B12 is nodig bij de isomerisatie (herschikking binnen dezelfde molecule), zoals in de reactie methylmalonyl-CoA naar succinyl-CoA. Deze reactie speelt een rol in het metabolisme van de vertakte aminozuren valine en isoleucine en van de vetzuren met oneven aantal C-atomen. Dit succinyl-CoA neemt dan deel aan de Krebscyclus om in het citraat, waarnaar de cyclus ook genoemd is, over te gaan na vijf tussenstappen. Maar dit is een ander verhaal…















Nog geen opmerkingen