‘Handige’ enzymen maken twee chirale centra
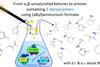
Gemakkelijk chirale moleculen maken is de droom van elke syntheticus. Francesco Mutti en zijn team gebruikten gemodificeerde enzymen om amines met twee stereocentra te maken in een één-pot-synthese, met hoge precisie en efficiëntie.
Het is geen geheim dat het bewerkstelligen van zuivere chiraliteit heel belangrijk én heel lastig is. Maar gelukkig zijn er enzymen; natuurlijke katalysatoren met, meestal, een zeer specifieke functie. In cellen werken ze heel goed samen, maar in het lab is het een ander verhaal.
‘Telkens als je een chemische transformatie met behulp van enzymen wilt doen waarbij je meerdere stappen tegelijkertijd moet uitvoeren, is de compatibiliteit een probleem’, zegt Francesco Mutti, universitair hoofddocent biokatalyse aan de Universiteit van Amsterdam. Maar onlangs hebben Mutti en zijn groep een belangrijke bijdrage geleverd aan een oplossing voor dit probleem.
Verder lezen?
Maak eenvoudig een gratis profiel aan.
- krijg toegang tot ons online archief met meer dan 10.000 artikelen over chemie, life sciences en procestechnologie;
- kijk webinars live mee of later terug, lees exclusieve online-only content en plaats reacties op artikelen;
- ontvang elke week onze nieuwsbrief C2Weekly in je mailbox met nieuws en ontwikkelingen zodat je altijd up-to-date bent.
Als lid van de KNCV, KVCV, NBV, of NVBMB heeft u onbeperkt toegang tot deze site, u kunt hier inloggen.










