Met kwantumchemische berekeningen analyseert een Utrechts-Amsterdams team de synthese, reactiviteit en bindingsvorming van nikkelcarbeencomplexen, staat in Chemistry – A European Journal.
Katalyse met goedkope overgangsmetalen is de droom voor veel chemici. Neem bijvoorbeeld nikkel. Vormt dat een dubbele binding met bijvoorbeeld koolstof (een carbeen), dan functioneert het als een belangrijk intermediair voor bijvoorbeeld cyclopropaansynthese. Maar zoals altijd helpt het enorm als je weet hoe een intermediair er precies uitziet, hoe het reageert én welk ligand het stabiliseert. Onderzoekers uit Utrecht en Amsterdam sloegen de handen ineen om de geheimen van het nikkelcarbeencomplex te ontrafelen.
‘Lang werd gedacht dat isoleerbare nikkelcarbeencomplexen niet mogelijk waren’, zegt Marc-Etienne Moret, universitair hoofddocent aan de Universiteit Utrecht. ‘Maar in de jaren 2000 liet de groep van Gregory Hillhouse zien dat je bij weinig liganden – twee in zijn geval – een situatie creëert waarin nikkelcarbeen stabiel is. Zijn fosfine-bidentaatligandcomplexen waren tot nu toe de enige voorbeelden. Daarom wilden wij weten: is het écht nodig om maar twee ligandbindingen te hebben of kan het ook met meer?’
Vierring
Die vraag stamt uit eerder onderzoek uit Morets groep. ‘We zijn al een tijdje bezig met de chemie van nikkelcarbenen en nikkelcyclobutaan, een vierring gevormd uit drie koolstofatomen en een nikkelatoom’, vertelt hij. ‘Ons langetermijndoel is namelijk om uit te zoeken of je met nikkelkatalysatoren olefinemetathese kunt doen.’ Dat gebeurt nu met vrij prijzige rutheniumcarbeencomplexen (zoals Grubb’s catalyst), maar voor nikkel is efficiënte olefinemetathese nog helemaal niet bekend, hoewel dat natuurlijk een stuk goedkoper zou zijn.
Postdoc Pablo Pérez-García en promovenda María Sansores-Paredes werken beiden in de groep van Moret aan de nikkelcomplexen. Moret: ‘Bij ons nikkelcyclobutaan vind je wel een soort van olefinemetathese, maar daar is het carbeen dat vormt nog steeds deel van de ring. Daarom probeerden we diezelfde coördinatie-omgeving te maken maar dan zonder dat het carbeen onderdeel van het ligand zou zijn. En dat lukte!’ Het resultaat was een verrassing volgens Moret. Er rezen meteen allerlei vragen: waarom werkt dit wel met drie fosfines en is het stabiel?
‘Toen klopte zijn groep bij ons aan’, zegt Pascal Vermeeren, universitair docent theoretische chemie aan de Vrije Universiteit Amsterdam. ‘Aan de VU kijken we heel veel naar verbindingen en structuren, ook van organometaalcomplexen, met kwantumchemie. Wat ik erg leuk vond aan dit project is dat María voor een periode naar onze groep kwam om de methodes te leren om in detail naar het bindingsmechanisme te kijken. We kunnen het wel zelf doen, maar ik vind dat we ook de nieuwe generatie wetenschappers breder moeten instrueren in al de verschillende aspecten van de chemie.’
Fenylvleugels
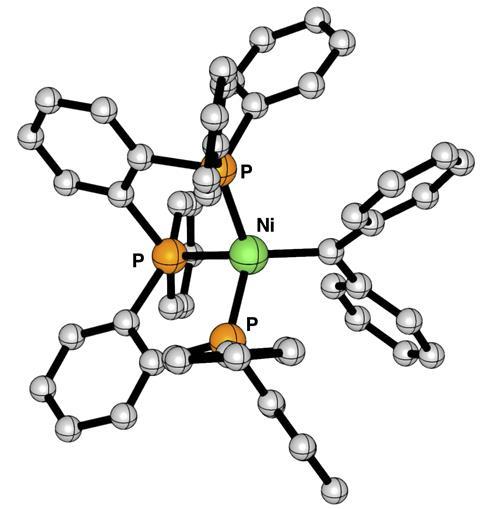
Sansores-Paredes bestudeerde eerst de Utrechtse complexen en vergeleek die toen met die van Hillhouse. ‘Beide nikkelcarbeencomplexen zijn stabiel, maar in de Utrechtse varianten zagen we dat de interactie zwakker is dan bij de bidentaatliganden’, legt Vermeeren uit. ‘Dat lijkt vooral te komen doordat het nieuwe systeem grote “fenylvleugels” heeft, die zorgen voor een sterische, repulsieve interactie met het inkomende carbeen.’
Ondanks dat de binding wat zwakker is en dus iets sneller zou moeten reageren dan de Hillhouse-varianten, is het molecuul in het algemeen niet zo reactief. ‘Juist omdat het zo beschermd is door die fenylvleugels, lukken reacties tot nog toe alleen maar met kleine moleculen als CO’, zegt Moret. ‘De hypothese is dat het nikkelcentrum nu niet echt toegankelijk is, dus onze volgende stap is om een complex met minder sterische bulk eromheen te maken.’
Met kwantumchemische berekeningen keken de onderzoekers dus eerst naar het verschil in interactie. ‘Het komt neer op een mismatch in orbitalen wanneer er drie fosfineliganden aan nikkel coördineren en dat zorgt ervoor dat de interactie minder stabiel is’, aldus Vermeeren.
Droomreactie
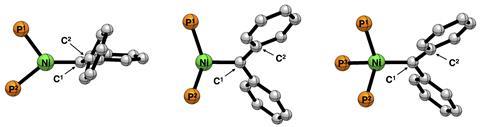
Vervolgens vroegen ze zich af wat het effect is van die derde fosfornikkelverbinding op het complex. ‘Daar komt in mijn ogen de schoonheid van de theoretische chemie naar voren’, zegt Vermeeren. ‘Met computermodellen kun je namelijk kijken naar dingen die synthetisch niet mogelijk zijn, maar wél inzicht geven.’ Daarvoor begonnen ze vanuit een simplistisch model van het Hillhouse-complex: nikkel met twee fosfines en een carbeen, zonder de rest van de liganden. ‘Dan verander je het model stapsgewijs naar het Utrechtse nikkelcarbeencomplex. Wat blijkt? De derde fosforbinding trekt elektronendichtheid weg van nikkel naar het ligand toe. Daardoor heb je minder repulsieve interactie langs de bindingsas met het carbeen.’
‘De droomreactie is om met nikkel olefinemetathese te doen’, zegt Moret. ‘Dit complex doet dat niet, maar op deze manier hebben we wel geleerd wat de mogelijkheden zijn.’ Op de korte termijn wil hij met zijn groep de complexen modificeren tot hij een reactiever carbeen heeft. Op de lange termijn leidt dat dan hopelijk tot olefinen. ‘Maar het meest interessante aan dit soort werk is het ontdekken van reacties die we niet verwachten. Dat is uiteindelijk de reden om zulke reactieve verbindingen te maken.’
Pérez-García, P.M., Sansores-Paredes, M.L.G. et al., Synthesis, reactivity and bonding analysis of a tetracoordinated nickel carbene, Chem. Eur. J. (2024), doi: 10.1002/chem.202403211




















Nog geen opmerkingen