Het Nederlandse onderzoeksconsortium Building a Synthetic Cell (BaSyC) is goed op weg. Nog even en alle nieuw ontwikkelde modules zijn klaar om samengevoegd te worden tot een (soort van) synthetische, levende cel. ‘We gaan een spannende tijd tegemoet.’
Net als het in elkaar zetten van een auto of een vliegtuig vanuit alle losse onderdelen. Zo noemt hoogleraar biochemie Bert Poolman van de Rijksuniversiteit Groningen (RUG) de bouw van een synthetische cel uit afzonderlijke componenten. Maar de analogie gaat niet helemaal op. ‘Bij een cel is het lastiger, want alles daarin is dynamisch, complex en plastisch. Zie dat maar eens na te bootsen. Maar al doende leer je.’
Vijf universiteiten (TU Delft, de Rijksuniversiteit Groningen, Universiteit Wageningen, Radboud Universiteit en VU Amsterdam) en onderzoeksinstituut AMOLF werken binnen het zwaartekrachtsprogramma BaSyC nu al zes jaar aan het ontwikkelen van al die onderdelen, de modules, en het combineren van de modules in een lipide-blaasje, de vesicle, om zo een minimale synthetische cel te verkrijgen.
Energieproductie

Uit welke modules moet zo’n zelfgemaakte cel bestaan? Ten eerste is een eigen energiecentrale onontbeerlijk. Die moet namelijk alle processen in de cel aandrijven. In natuurlijke cellen zijn er twee vormen van energie voorradig: een elektrische potentiaal en het brandstofmolecuul ATP. Voor die eerste heeft de groep van Poolman een simpele module bedacht. ‘Een eiwit in het membraan van de vesicle neemt dicarbonzuren op, waarna een enzym die decarboxyleert tot koolstofdioxide, waarbij protonen worden verbruikt. Zo ontstaat een elektrische potentiaal over het membraan. Dat geeft de energie die is nodig voor het naar binnen pompen van voedingstoffen en het uitscheiden van afvalstoffen.’ Een van die voedingsstoffen is arginine. Dit aminozuur is belangrijk voor de ATP-productie. ‘Uit eerder onderzoek kenden we al de benodigde reacties’, geeft Poolman aan, die met UG-collega Matthias Heinemann samenwerkte op dit onderdeel. Poolman: ‘Arginine wordt in drie stappen omgezet tot ornithine. In de derde stap wordt ATP uit ADP gevormd. Het geheel bevindt zich in een mini-compartiment dat de brandstof voor de uiteindelijke cel moet leveren.’
Dit proces van ATP-productie liep gesmeerd. Zo gesmeerd zelfs dat al de voorraad ADP in de cel opraakte en de reactie tot stilstand kwam. ‘Het gevolg was dat de arginine-afbraak verder ging via een futiele route, waarbij geen ATP ontstaat, maar de cel wel verzuurt en enzymen hun activiteit verliezen.’ De synthetische cel maakt dus energie, maar moet dit vervolgens wel gebruiken om te voorkomen dat ongewenste neveneffecten ontstaan.
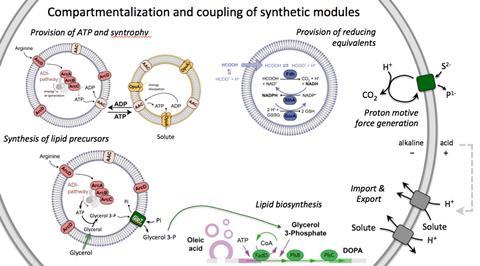
Voor het verbruik van de ATP werkt Poolman samen met de groep van weer een andere Groningse collega, Arnold Driessen, aan membraanvorming. Dat is nodig voor de groei van de cel. ‘Eerst wordt het vetzuur oleïnezuur binnengebracht in een aparte module’, legt Poolman uit. ‘Verder is glycerol-trifosfaat nodig, dat vanuit de ATP-productie komt. Het ATP zelf is nodig voor de koppeling van de twee verbindingen tot een eenvoudig lipide, DOPA [dioleoylfosfatidinezuur, red.]. Die wordt vervolgens in meerdere stappen omgezet tot het bekendere membraanbestanddeel DOPG [dioleolyfosfatidylglycerol, red].’ Het principe werkt, maar op dit moment worden die lipiden alleen nog maar aan de binnenkant van het blaasje gevormd. Poolman: ‘We hebben nu nog een transportsysteem nodig dat de geproduceerde lipiden naar de andere helft van de membraan brengt, zodat we een stabiele lipide-dubbel membraan krijgen, net zoals bij natuurlijke cellen.’

Operon
De energiemodules van Poolman en collega’s functioneren, maar het kan natuurlijk altijd beter. In de natuur verloopt deze fine tuning via evolutie. Kunnen wij hetzelfde doen? Jazeker, denkt John van der Oost, hoogleraar microbiologische genetica aan Wageningen Universiteit. Eerst werkte Van der Oost met zijn team aan een testcase in een natuurlijke cel: een stukje synthetisch genoom waarop RNA-polymerase staat gecodeerd. Dit enzym is belangrijk voor het overschrijven van DNA. Van der Oost: ‘In tegenstelling tot genen die coderen voor veel andere bacteriële eiwitcomplexen, liggen de genen van RNA-polymerase in Escherichia coli verspreid over het hele genoom. Wij hebben wij al die genen kunnen combineren tot één functioneel gencluster, of operon. Vervolgens hebben we in meerdere rondes van celdeling steeds die cellen geselecteerd die het snelst groeiden. Gestuurde evolutie dus. Het resultaat was het best mogelijke operon. Deze werkwijze vormt dus een goed voorbeeld van hoe we het genoom van een synthetische cel zouden kunnen opbouwen.’
Vervolgens bood Van der Oost zijn diensten van het optimaliseren van modules via de evolutionaire weg aan bij de andere partners van het consortium. Zijn eerste klus: het Groningse ATP-productieproces. ‘Voor de vier genen die hierbij betrokken zijn, hebben we verschillende combinaties en sequenties uitgeprobeerd om te bepalen hoe we de beste expressie konden verkrijgen’, vertelt Van der Oost. ‘Uiteindelijk hadden we een goed werkend operon in handen.’
Maar is dat operon, en de daaruit volgende enzymen, goed genoeg om de toekomstige synthetische cel van alle benodigde ATP te voorzien? ‘Ik denk dat het lastig gaat worden’, geeft Van der Oost aan. ‘Maar uit experimenten bij E. coli, waar we het operon inbouwden, blijkt dat de module er wel voor zorgt dat de cel goed groeit in een kweekmedium waar de cel normaliter moeite mee zou hebben.’ De volgende opdracht voor Van der Oost en zijn groep ligt alweer klaar: de operons bouwen voor eiwitten die de celcyclus en celdeling reguleren. Dat gaat hij doen in samenwerking met partners van onderzoeksinstituut AMOLF.
Insnoeren
Iemand die ook aan celdeling werkt, en dan met name aan de groei en deling van het lipide-celmembraan, is hoogleraar bionanoscience Gijsje Koenderink van de TU Delft. Net als in Groningen worden ook in Delft membranen gemaakt, maar haar collega Christophe Danelon gaat nog een stapje verder. ‘Wij werken niet met opgezuiverde enzymen, maar met een synthetisch genoom waarop alle benodigde enzymen gecodeerd zijn voor de synthese van lipiden.’ Dit systeem werkt, maar er is nog wel een beperking, geeft Koenderink aan. ‘Een cel moet heel veel extra membraan aanmaken om te kunnen delen in twee dochtercellen die even groot zijn als de oorspronkelijke cel. Maar zoveel membraan kunnen we nu nog niet maken.’

In plaats daarvan hebben Koenderink en collega’s een tussenstap bedacht: membraanfusie. Dat werkt volgens haar als volgt. ‘Je voegt aan een synthetische vesicle kleine blaasjes toe met DNA-strengen die complementaire DNA-strengen op de synthetische cel herkennen, binden en samensmelten. Hierdoor kun je het celmembraan naar believen laten groeien.’ En dan tenslotte nog die celdeling. Dat is de grootste uitdaging van haar werk, stelt Koenderink. ‘Je moet dat membraan heel precies in het midden insnoeren met behulp van een “ring”. In de natuur gebeurt dat met behulp van het cytoskelet, een netwerk van actinedraden die krachten uitoefenen op het celmembraan.’
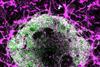
Koenderinks onderzoek is erop gericht om uit te vinden hoe actine-draden zichzelf organiseren tot een ring. ‘Sleutel daarvoor is dat de actinedraden vanaf het membraan naar binnen moeten groeien en niet binnen in het cytosol, legt ze uit. ‘Dit leggen we op door eiwitten aan het membraan te koppelen die de groei van nieuwe actinedraden katalyseren. Ook moet er voldoende ATP aanwezig zijn, zodat de draden actief polymeriseren en depolymeriseren, en daarmee krachten uitoefenen.’
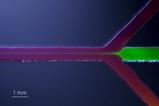
En nu nog de cel laten weten waar het midden is. Ook daar heeft Koenderink een truc voor bedacht. ‘We gaan de vesicles door microfluïdische chips trekken. Die chips bevatten kanaaltjes met inkepingen. Tijdens de passage ontstaan er dan vervormingen in het midden van het plasmamembraan. Vanaf daar kan de ‘cel’ dan gaan insnoeren. We zijn nu bezig met testen of het werkt.’ De volgende stap is ook al duidelijk. Uiteindelijk moet de cel helemaal zonder hulp gaan delen. Koenderink werkt hiervoor samen met haar Delftse collega-hoogleraar én trekker van het BaSyC-programma Marileen Dogterom. Zij werkt aan microtubuli, een ander onderdeel van het cytoskelet dat onder meer fungeert als ‘kompas’ voor de cel.
Autonoom?
Genoeg uitdagingen dus nog de komende jaren. Het gehele BaSyC-project loopt nog tot 2027, maar eigenlijk is dat volgens alle drie de onderzoekers te weinig tijd om een volledig autonome synthetische cel op te leveren. Waar zijn ze dan wel tevreden mee? Poolman: ‘Als we onze energiecentrale kunnen laten werken vanuit een synthetisch genoom, zou ik persoonlijk al heel blij zijn.’ Datzelfde geldt voor de modules van Koenderink. ‘Pas met een synthetisch genoom kan een cel autonoom groeien en delen’, geeft ze aan.
En tenslotte moeten al die verschillende modules, van ATP-productie tot membraangroei en celcyclus-processen met elkaar gaan samenwerken. ‘Dat is nog wel de grootste uitdaging’, stelt Van der Oost. Maar zo is het leven ook ooit begonnen, geeft Poolman aan. ‘Al die verschillende functies zijn ooit ontstaan en samengekomen in de eerste protocel die vervolgens verder is geëvolueerd. Op die manier kunnen wij ook een synthetische cel gaan bouwen. We gaan absoluut een spannende tijd tegemoet.’
Waarom een synthetische cel?
Waarom wil het Building a Synthetic Cell (BaSyC)-consortium eigenlijk een synthetische cel bouwen? Er zijn twee redenen volgens Bert Poolman. ‘De eerste is het begrijpen van de complexiteit van de levende cel. In plaats van die cel stap voor stap te ontrafelen, wat erg lastig is, proberen wij een cel beetje bij beetje op te bouwen en daarbij inzichten op te doen.’
De tweede reden omvat de directe toepassingen van zo’n synthetische cel. Poolman: ‘Onze energiemodule, die ATP produceert, zou kunnen worden ingezet om nanopore-DNA-sequencing efficiënter te maken.’ Ook kun je volgens Gijsje Koenderink denken aan microbiële productie van eiwitten voor voeding of therapeutische antilichamen. ‘Normaal worden natuurlijke cellen aangepast om een bepaald product te maken, maar een synthetische cel is al from scratch ontworpen voor een specifieke toepassing. Dat zou weleens veel beter kunnen werken.’ En, besluit, Poolman: ‘Naarmate we meer leren, zullen er meer mogelijkheden komen.’





![network_with_colored_proteins_[11007]](https://d3rlrdre72yelp.cloudfront.net/Pictures/100x67/2/8/2/15282_network_with_colored_proteins_11007_318021.jpg)
Nog geen opmerkingen